本报讯 中国科大生命科学与医学部周丛照教授和陈宇星教授课题组,利用单颗粒冷冻电镜技术解析了三种不同状态的硝酸盐/亚硝酸盐ABC转运蛋白NrtABCD(缩写为NRT)的三维结构,包括结合底物硝酸根NO3-、结合Mg2+-ATP以及结合信号蛋白PII的结构。基于结构和生化分析以及生理实验,作者阐明了一种新型ABC转运蛋白的底物识别模式和转运循环,以及PII如何通过响应不同的效应分子进而精细调控NRT转运活性的分子模型。相关研究成果3月8日在线发表在学术期刊《美国科学院院报》上。
作者解析了NrtBCD三种不同状态的三维结构。其中,结合底物硝酸根的NrtBCD-NO3-结构呈现向内开口(inward-facing)的构象,TMD中存在一个由结合硝酸根的疏水腔和富含精氨酸残基的亲水腔组成的连续的底物转运通道,负责底物的进入和释放。在结合Mg2+-ATP的NrtBCD-ATP结构中,ATP的结合引发NBD相互靠近,导致TMD发生构象变化,底物转运通道被封闭,形成封闭的向外开口(outward-facing occluded)的构象。NrtBCD-PII复合物结构采用了一种完全不对称的抑制型构象(图1)。与以前报道的PII通过T-loop结合靶蛋白的方式不同,NrtBCD-PII中的PII通过核心结构域中的T-loop基部、B-loop和C-loop等元件同时结合NrtC的NBD和CRD结构域,代表了一种新的相互作用模式。
作者通过结构分析结合生化生理实验提出了PII通过调控NRT活性进而维持蓝细菌碳氮平衡的分子模型:在高N/C比时,PII通过与NrtC直接结合进而与NRT形成复合物,将NRT锁定为抑制型向内开口(inhibited inward-facing)的构象,同时跨膜区的底物转运通道收窄,抑制了NRT的硝酸盐/亚硝酸盐转运活性。而在低N/C比时,细胞内的α-酮戊二酸(2-OG)累积,此时2-OG结合PII并导致PII发生构象变化,使其从NrtC上解离下来,NRT转运活性得以恢复,向胞内转运硝酸盐/亚硝酸盐,维持碳氮平衡。
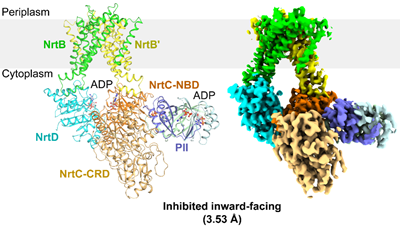
NrtBCD-PII复合物的三维结构
中国科大博士生李波为论文第一作者,中国科大周丛照教授、江永亮副教授和陈宇星教授为共同通讯作者。
(生命科学与医学部)